凱氏定氮儀測(cè)定針劑中真蛋白含量
1 前言
眾所周知,凱氏定氮法所測(cè)定的氮包括有機(jī)態(tài)的氮以及無(wú)機(jī)態(tài)的氮。而對(duì)于一些針劑等需要測(cè)定真蛋白的樣品而需要進(jìn)行特殊的處理,將樣品中的非蛋白氮進(jìn)行測(cè)定,其差值則為真蛋白氮,從而可以計(jì)算得到真蛋白值,這里我們用到的是鎢酸沉淀法。
2 實(shí)驗(yàn)部分
2.1原理
根據(jù)《中國(guó)藥典2015版》中的規(guī)定。采用鎢酸沉淀法將真蛋白進(jìn)行沉淀,測(cè)得非蛋白氮含量。
2.2 儀器與試劑、器具
2.2.1 K1100F全自動(dòng)凱氏定氮儀(濟(jì)南海能儀器股份有限公司)。
2.2.2 SH420F石墨消解儀(濟(jì)南海能儀器股份有限公司)。
2.2.3 硼酸 分析純,質(zhì)量分?jǐn)?shù)2%。
2.2.4 氫氧化鈉 分析純,質(zhì)量分?jǐn)?shù)40%。
2.2.5 亞甲基藍(lán)-甲基紅混合指示劑 將亞甲基藍(lán)乙醇溶液(1g/L)與甲基紅乙醇溶液(2g/L)按1:1體積比臨時(shí)混合搖勻備用。
2.2.6 鎢酸鈉 分析純 質(zhì)量分?jǐn)?shù)10%
2.2.7 稀硫酸 0.33mol/L
2.2.8 硫酸標(biāo)準(zhǔn)酸 0.1mol/LH+
2.2.9氯化鈉 分析純 質(zhì)量分?jǐn)?shù)0.9%
2.2.10 移液管
2.3 實(shí)驗(yàn)步驟
2.2.1總氮樣品制備:精密量取供樣品5ml,用0.9 %氯化鈉溶液定量稀釋至100ml,制成每 lml中含氮量約 lmg的溶液,精密量取 lml,作為總氮供試品溶液進(jìn)行測(cè)定 。
2.2.2非蛋白樣品制備:精密量取2ml樣品, 置20ml量瓶中,加水14ml,加10 %鎢酸鈉溶液2.0ml,0.33mol/L硫酸溶液2.0ml,加水至刻度,搖勻,靜置30分鐘,濾過(guò),取濾液5ml。
2.2.3取樣:消化管中各加入0.3g稀硫酸鉀,10滴30%的硫酸銅溶液。
2.2.4消解:利用石墨消解爐進(jìn)行消解,將消化管放在石墨爐上,蓋上排
氣罩,連接廢氣吸收系統(tǒng),消化完畢后,將消化管取下冷卻至室溫。消化過(guò)程采用曲線升溫模式,設(shè)置參數(shù)如下:消化過(guò)程采用曲線升溫模式,設(shè)置參數(shù)如下:
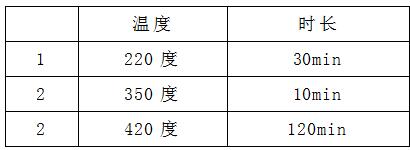
注意:如果加大取樣量,需要緩慢升溫。再次升溫以樣品不冒泡沖樣為準(zhǔn)。如果消解過(guò)程中樣品劇烈沸騰冒泡,立即停止加熱。
2.3.5 定氮儀設(shè)置程序如下:
稀釋水:30ml
硼酸:25ml
蒸餾時(shí)間:5min
2.3.6 儀器自動(dòng)滴定并給出結(jié)果。
3 結(jié)果與討論
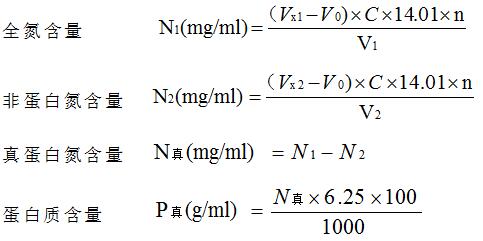
式中:C-標(biāo)準(zhǔn)酸摩爾濃度(mol/L)
V0-空白樣滴定標(biāo)準(zhǔn)酸消耗量(mL)
Vx1-全氮樣品滴定標(biāo)準(zhǔn)酸消耗量(mL),精確到小數(shù)點(diǎn)后四位
Vx2-全氮樣品滴定標(biāo)準(zhǔn)酸消耗量(mL),精確到小數(shù)點(diǎn)后四位
n-稀釋倍數(shù)
注意:
(1)如果樣品蛋白質(zhì)含量超過(guò)10%,應(yīng)加大稀釋倍數(shù)。10%鎢酸鈉溶液及稀硫酸溶液用量相應(yīng)的按比例增加,使溶液中鎢酸濃度保持1%。
(2)全氮含量以及非蛋白氮含量可用同一空白體積。





