電位滴定法檢測水中的COD的含量
1 前言
在自然界的循環(huán)中,水中的還原性物質,特別是有機化合物在生物氧化降解過程中消耗溶解氧而造成水體氧的缺損,溶解氧的缺損會破壞環(huán)境和生物群落的生態(tài)平衡,引起水質惡化,甚至發(fā)生溶解氧消耗殆盡,厭氧菌滋生,造成水體變黑發(fā)臭。這就需要針對水中的有機物進行檢測。由于有機化合物有數(shù)百萬種,難以分別定性定量檢測。在實踐的基礎上,環(huán)境分析學家尋求到另一種途徑,確定一種綜合指標,利用有機化合物的還原物質,將消耗的量作為一項新的指標,這樣化學需氧量和生化需氧量就因運而生了。由于生物氧化是一個緩慢的過程,一個月的時間也只能氧化到70%作用,這對污染治理的實際操作就顯得滯后,分析化學家們將生物氧化的碳化部分定為五日生化需氧量,雖然在某種程度上縮短了時間,但仍顯得漫長。在這種情況下就出現(xiàn)了化學需氧量。
化學需氧量是指水體中易被強氧化劑(一般采用重鉻酸鉀)氧化的還原性物質所消耗的氧化劑的量,結果折成氧的量(以mg/L計)。它是表征水體中還原性物質的綜合指標。除特殊水樣外,還原性物質主要是有機化合物,組成有機化合物的碳,氮,硫,磷等元素往往處于較低價的氧化價態(tài)。
2 儀器與試劑
2.1 儀器

T960自動電位滴定儀,Hamilton鉑復合電極
Tank全自動消解儀
2.2 試劑
溶液均用一級水配制,配制方法見附錄。
硫酸亞鐵銨溶液(0.05mol/L),重鉻酸鉀溶液(0.25mol/L)、硫酸銀-硫酸溶液(10g/L),濃硫酸、實驗用一級水。
3 實驗方法
3.1 實驗步驟
(1)硫酸亞鐵銨的標定
吸取5mL重鉻酸鉀溶液(0.25mol/L),加入50mL水,緩慢加入15mL濃硫酸,冷卻后加入3滴試亞鐵靈指示劑,用硫酸亞鐵銨溶液滴定至終點。
(2)樣品測試
稱取試樣10mL,用一級水稀釋定容于250mL容量瓶中。吸取10mL稀釋液于消解罐中,準確加入5mL重鉻酸鉀溶液(0.25mol/L),再加入15mL硫酸銀-硫酸溶液(10g/L),開始消解。
待消解罐冷卻后,將消解后的溶液轉入滴定杯中,用30mL一級水清洗消解罐壁,并將清洗液一并轉入滴定杯中。冷卻后用標定好的硫酸亞鐵銨滴定至終點。空白樣品用10mL一級水代替。
3.2 儀器參數(shù)
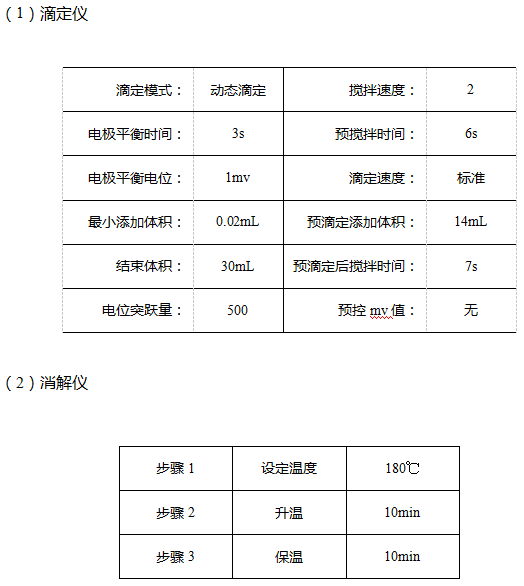
4 結果與討論
4.1 實驗結果
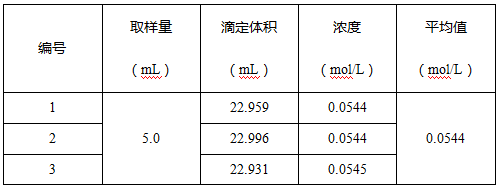
(2)水樣
空白體積:22.434mL
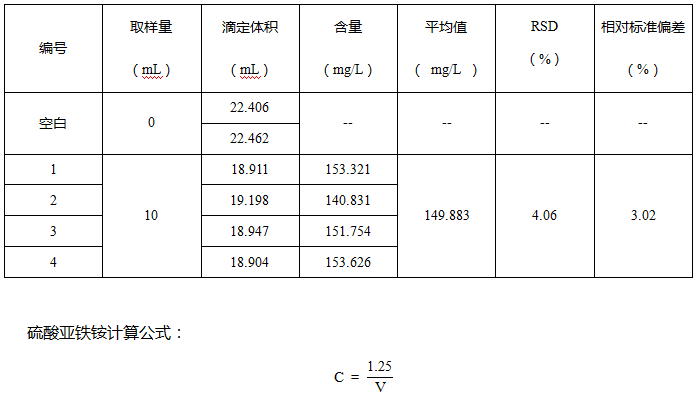
式中:
C --為硫酸亞鐵銨的含量,單位為摩爾每升(mol/L);
V --滴定時消耗硫酸亞鐵銨溶液的體積,單位為毫升(mL)。
化學需氧量計算公式:
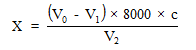
式中:
X --為試樣中化學需氧量的含量,單位為毫克每升(mg/L);
V1 --樣品試驗消耗硫酸亞鐵銨溶液的體積,單位為毫升(mL);
V0 --空白試驗消耗硫酸亞鐵銨溶液的體積,單位為毫升(mL);
c --硫酸亞鐵銨溶液的濃度,單位為摩爾每升(mol/L);
V2 --水樣體積,單位為克(g);
8000 --為1/4的O2摩爾質量以mg/L為單位的換算值。
4.2 滴定圖譜
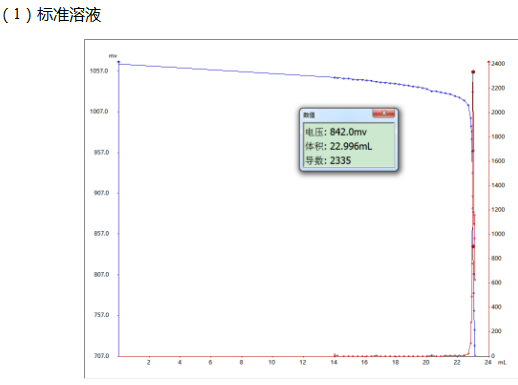
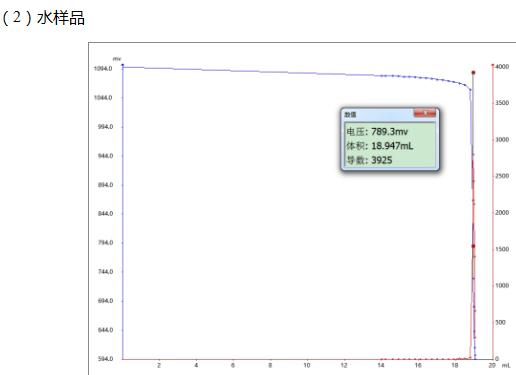
4.3 結論
相對標準偏差為3.02%,符合文獻對于精密度的要求。同時也證明了微波消解儀對于樣品前處理的可行性,可以進行推廣。
參考文獻
[1]HJ/T828-2017水質 化學需氧量的測定 重鉻酸鉀法[S].
附錄
1)硫酸亞鐵銨溶液(0.05mol/L):稱取9.75g硫酸亞鐵銨,溶解于一級水中,加入10mL濃硫酸,待溶液冷卻后用一級水稀釋至500mL。
2)重鉻酸鉀溶液(0.25mol/L):準確稱取在105℃烘箱中干燥至恒重的重鉻酸鉀12.258g,溶解于一級水中,定容到1L。
3)硫酸銀-硫酸溶液(10g/L):稱取2.5g硫酸銀,用硫酸定容至250mL。搖勻,使用前小心搖動。





