電位滴定法測(cè)定混酸中硫酸硝酸含量
1 前言
硫酸硝酸混合而成的混酸在生產(chǎn)上主要用作反應(yīng)溶劑,作為相似的極性溶劑,硫酸和硝酸可以像和水一樣互相形成氫鍵,從而放熱。硝化反應(yīng)是指向有機(jī)化合物分子中引入硝基的過(guò)程,常用的硝化劑主要是濃硝酸,發(fā)煙硝酸,以及濃硝酸和濃硫酸制成的混酸,當(dāng)被硝化物在反應(yīng)溫度下為固體而且容易被磺化時(shí)可采用有機(jī)溶劑中的硝化,混酸組成是影響硝化能力的主要因素,對(duì)于每個(gè)具體的硝化過(guò)程,其混酸組成都要通過(guò)實(shí)驗(yàn)來(lái)確定它們的適宜范圍。由于濃硝酸的易揮發(fā)性,很難直接測(cè)定其含量,故采用酸堿滴定的方法來(lái)分別測(cè)定混酸中總酸含量和硫酸含量,根據(jù)差值計(jì)算出硝酸含量。
2 儀器與設(shè)備
2.1 儀器
T960電位滴定儀,pH復(fù)合電極。
2.2 試劑
甲醛溶液(1+1),氫氧化鈉溶液(0.5mol/L)。
3 實(shí)驗(yàn)方法
3.1 實(shí)驗(yàn)步驟
總酸測(cè)定:取0.5g混酸樣品于滴定杯中,加入70mL水,攪拌均勻后,用氫氧化鈉滴定液滴定至終點(diǎn),同時(shí)作空白試驗(yàn)。
硫酸測(cè)定:取0.5g混酸溶液于滴定杯,放入油浴中,加入10滴甲醛溶液(1+1),在120℃油浴下保溫20min,以除去樣品中的硝酸,后取出加入70mL水,攪拌均勻后,用氫氧化鈉滴定液滴定至終點(diǎn),同時(shí)作空白試驗(yàn)。
3.2 參數(shù)設(shè)置
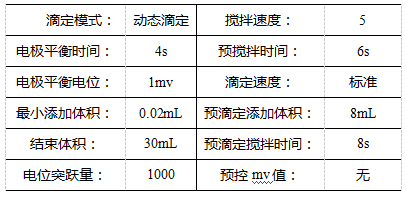
4 結(jié)果與討論
4.1 實(shí)驗(yàn)結(jié)果
空白體積:0.025mL
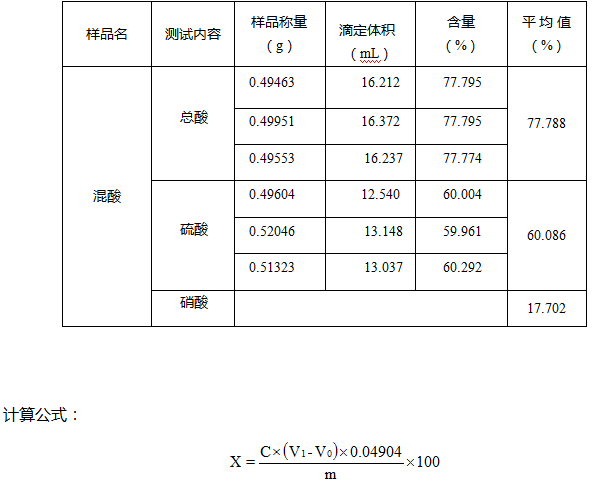
式中:
X -- 樣品中混酸/硫酸的含量,單位為(%);
V1 -- 樣品消耗氫氧化鈉溶液的體積,單位為毫升(mL);
C -- 氫氧化鈉溶液的濃度,單位為摩爾每升(mol/L);
V0 -- 空白消耗氫氧化鈉溶液的體積,單位為毫升(mL);
m -- 樣品的質(zhì)量,單位為(g);
0.04904 -- 硫酸的毫克當(dāng)量數(shù),單位為克(g)。
4.2 圖譜
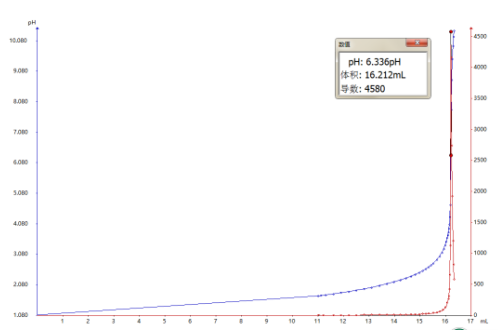
4.3 結(jié)論
取平行測(cè)試結(jié)果的算術(shù)平均值為測(cè)定結(jié)果,可以看出先測(cè)量總酸硫酸含量再利用差值計(jì)算硝酸含量的方法可行,且實(shí)驗(yàn)重復(fù)性良好。
注意事項(xiàng)
由于硝酸易揮發(fā),為保證實(shí)驗(yàn)的準(zhǔn)確性實(shí)驗(yàn)過(guò)程中應(yīng)用減量法稱取混酸樣品。





